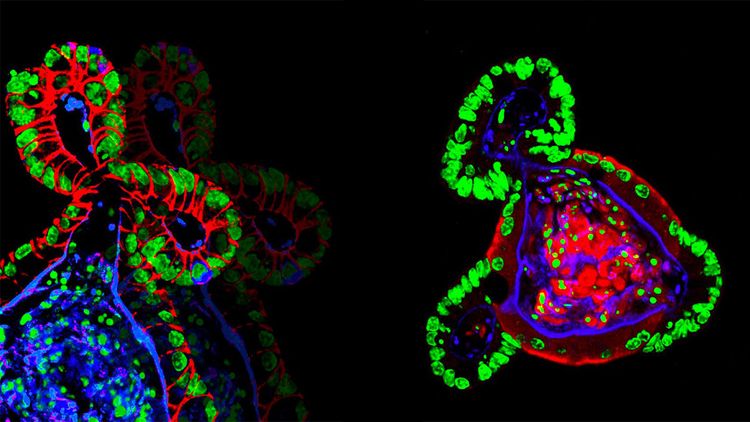
Aufnahme von Darmorganoiden mithilfe der Fluoreszenzmikroskopie: Die aus adulten Stammzellen gezüchteten Gewebemodelle sollen in Zukunft eine ganze Reihe von Anwendungen in der Wirkstoffentwicklung und der personalisierten Medizin finden.
Venedig – Eine neue Leber aus dem 3D-Drucker? Warum nicht. Die entsprechenden Zellen werden im Labor vermehrt und als Teil einer gelartigen Flüssigkeit dann Schicht für Schicht zum Gewebe eines maßgeschneiderten Organs geformt und in den Körper des Patienten transplantiert. Und damit noch nicht genug: Irgendwann sollen mithilfe derartiger Technik gar synthetische Lebewesen aus dem Bioprinter kommen.
Die Visionen und Hoffnungen, die um Bioingenieure kreisen, die ganze biologische Systeme gezielt herstellen, sind heute selbstverständlicher Teil von Zukunftsentwürfen – egal ob sie von wissenschaftlich orientierten Futurologen kommen oder in TV-Serien wie Westworld verwoben sind, in der die menschlich geformten Körper von Robotern aus dem Bioprinter kommen.
Der wichtigste Ausgangspunkt der Vorstellungen von reproduzierbaren Körpern liegt in der Stammzellenforschung. Seit den 1980er-Jahren werden aus diesem Feld bahnbrechende Erfolge vermeldet. Embryonale Stammzellen wurden identifiziert, die in der frühen Phase der Entwicklung eines Organismus auftreten und sich in alle möglichen Körperzellen verwandeln können. Adulte Stammzellen wurden isoliert, die während der ganzen Lebenszeit eines Organs vorhanden sind und sich nur in bestimmte Zelltypen entwickeln. Schließlich konnten Körperzellen erwachsener Menschen zu sogenannten induzierten pluripotenten Stammzellen reprogrammiert werden, die embryonalen Stammzellen gleichen.
Bereits 2009 konnte die Herstellung sogenannter Organoide vermeldet werden: Dem niederländischen Molekularbiologen Hans Clevers gelang es, adulte Stammzellen im Labor so zu vermehren, dass sich wenige Millimeter große "Miniorgane" herausbildeten: eine Erfindung, die zwar keine Ersatzleber, aber doch ein weites Feld an Anwendungen in Wirkstoffentwicklung und personalisierter Medizin möglich macht.
"Einer unserer ersten erfolgreichen Einsätze von Organoiden liegt im Feld der zystische Fibrose. Zum ersten Mal gibt es ein Medikament, das den Patienten eine normale Lebensspanne ermöglicht", sagt Robert Vries im Rahmen der kürzlich in Venedig stattgefundenen Verleihung des Erfinderpreises durch das Europäische Patentamt. Vries forschte gemeinsam mit Hans Clevers an den Miniorganen und steht heute – gemeinsam mit Clevers und anderen Wissenschaftern – der niederländischen Non-Profit-Organisation Hubrecht Organoid Technology (HUB) vor, die die Aufgabe hat, die Grundlagenforschung an der Universität Utrecht in Anwendungen zu überführen.
Zystische Fibrose, auch Mukoviszidose genannt, ist eine vererbte Stoffwechselerkrankung, die die Sekrete von Drüsen im menschlichen Körper verändert und zu Funktionsstörungen in verschiedenen Organen führt. An die 2000 Mutationen mit jeweils unterschiedlichen Krankheitsausprägungen sind bekannt. "Wir hatten ein Medikament, das bei manchen Patienten sehr gut wirkte, bei anderen aber überhaupt nicht", blickt Vries zurück. "Mithilfe der Organoide können wir vorhersagen, ob ein Patient auf die Behandlung ansprechen wird." Die Forscher konnten beweisen, dass das Gewebe aus dem Labor tatsächlich die Organfunktion eines Patienten repräsentiert.
Krebsorganoide
Einerseits sollen Organoide aus Proben von Patienten der Diagnostik dienen. Andererseits sollen ganze Arsenale an Organoidmodellen der Pharmaindustrie helfen, neue Behandlungen systematisch testen und entwickeln zu können. An Vries' Institution wird nun etwa daran gearbeitet, Krebsorganoide im Labor wachsen zu lassen.
Was Clevers und Kollegen als Erste bei Darmgewebe zeigten, gelang einer Forschergruppe um Jürgen Knoblich am Institut für Molekulare Biotechnologie (IMBA) der Österreichischen Akademie der Wissenschaften (ÖAW) im Jahr 2013 mit Gehirngewebe. Die Gehirnorganoide, die aus menschlichen Stammzellen gewonnen wurden, können verwendet werden, um etwa neurologische Erbkrankheiten zu erforschen. Tiermodelle können der Komplexität des menschlichen Gehirns nicht in dem Ausmaß gerecht werden, wie die im Labor entstandenen Modelle.
Auf Basis dieser Forschung konnten vor kurzem erstmals Gehirnorganoide mit biotechnologischen Methoden kombiniert werden. In einer in Nature Biotechnology publizierten Studie, an der auch Knoblich beteiligt war, gab ein internationales Forscherteam den Zellverbänden, die sich aus den Stammzellen entwickelten, eine formgebende Struktur mit: Die Zellen bevölkern ein Gerüst aus Polymerfäden. Das führt zu einer Anordnung, die dem embryonalen Gehirn besser entspricht als bisherige Organoide.
Zelltherapie
Die Herstellung von Organgewebe aus Stammzellen stößt die Tür zu neuen Behandlungen weit auf. Einer der wichtigsten Anwendungsbereiche wird in den kommenden Jahrzehnten in der Zelltherapie liegen. Aus den Organoiden sollen sich Ersatzzellen gewinnen lassen, die in ein menschliches Organ transplantiert werden können. Für Robert Vries liegt die Aussicht, eine Leber mithilfe von Zellen aus Organoiden behandeln zu können, in greifbarer Nähe. "Wir investieren sehr viel in diesen Bereich. Ich glaube nicht, dass es bereits in fünf Jahren möglich sein wird. Wenn es in 15 Jahren aber auch noch nicht gelingt, wäre ich etwas enttäuscht", umreißt der niederländische Wissenschafter die Aussichten.
Und wie sieht es nun mit der Perspektive aus, vollständige Organe im Labor heranzuzüchten? "Wir kennen nun die Wachstumsfaktoren, die wir brauchen, damit verschiedene Stammzellen so wachsen, wie sie es im Körper tun würden. Aber wir haben durch die Stammzellenforschung auch erkannt, dass wir die Interaktion zwischen verschiedenen Zelltypen in einem Organ nicht wirklich verstehen", sagt Vries. Dieses Verständnis wäre aber eine Grundvoraussetzung, um tatsächlich Organe reproduzieren zu können. "Versucht man, verschiedene Zelltypen zu verbinden, funktioniert das nicht. Die einen wachsen, die anderen nicht", sagt der Forscher. Vries' Fazit: "Wir verstehen kein Organ so gut, dass wir es nachbauen könnten." Das wird wohl noch längere Zeit so bleiben. (Alois Pumhösel, 25.8.2017)