Wenn die Versorgung des Gehirns mit Blut unterbrochen wird, geht es ganz schnell. Ohne sofortige Gegenmaßnahmen kommt es binnen Sekunden zum Zusammenbruch der Sauerstoffversorgung, Bewusstlosigkeit setzt ein, und eine irreversible Kaskade von Stoffwechselreaktionen nimmt ihren Lauf. Die Energiespeicher für die Nervenaktivität erschöpfen sich innerhalb von Minuten, die Zellkommunikation reißt ab, die Zellen sterben. Schließlich tritt der Hirntod ein.
Eine aktuelle Studie im Fachblatt "Nature" zieht nun einige Annahmen zum rasanten, unumkehrbaren Gehirnverfall in Zweifel und liefert Hinweise darauf, dass manche Zellfunktionen im Gehirn noch geraume Zeit nach dem Tod wiederhergestellt werden könnten. Wie die Forscher um Nenad Sestan von der Yale School of Medicine in New Haven berichten, konnten sie Schweinegehirne ganze vier Stunden nach dem Tod der Tiere stabilisieren, den Zelltod verlangsamen und sogar wieder vereinzelte synaptische Aktivitäten feststellen.
Künstlicher Durchblutungsapparat
Die Wissenschafter betonen, dass zu keinem Zeitpunkt Hirnströme gemessen werden konnten, die auf eine normale Funktion oder gar ein Bewusstsein hingedeutet hätten. Aus ethischen Gründen wurde eine solche Möglichkeit im Rahmen der Studie aber auch von vornherein medikamentös ausgeschlossen. "Es handelt sich sozusagen nicht um ein lebendes Gehirn, aber um ein zellulär aktives Gehirn", sagte Sestan.
Möglich wurde die Studie dank eines künstlichen Durchblutungssystems, das die Forscher Brainex nennen. Vereinfacht gesagt besteht das System aus zwei Komponenten: erstens aus einem Blutersatz, bei dem es sich um eine spezielle zellschützende Nährstofflösung handelt. Dieses Kunstblut wird zweitens mit einem Durchblutungsapparat aus Pumpen, Filtern und Temperaturregulatoren, der den Blutkreislauf imitiert, durch die Blutgefäße von chirurgisch entnommenen Gehirnen geleitet.
Spontane Aktivität
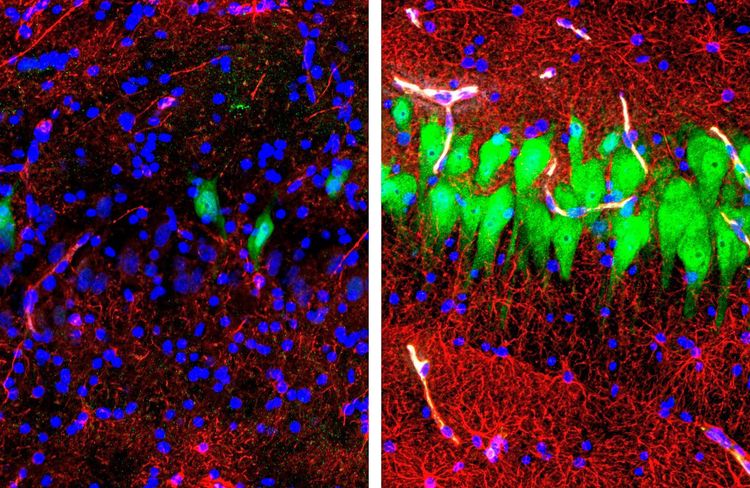
Für ihre Studie verbanden die Forscher insgesamt 32 Gehirne von Schweinen, die in einem Schlachthof zur Lebensmittelherstellung getötet worden waren, mit dem Brainex-System. Die künstliche Durchblutung wurde vier Stunden nach dem Tod der Tiere gestartet und sechs Stunden lang durchgeführt. "Zu diesem Zeitpunkt waren dramatische Veränderungen feststellbar", berichtete Sestan. Den Forschern war es gelungen, die Sauerstoffversorgung wieder zu gewährleisten und den zellulären Metabolismus anzukurbeln.
In der Folge stabilisierte sich die Zellarchitektur, das Absterben von Zellen wurde reduziert, und es ließen sich Reaktionen auf medikamentöse Wirkstoffe feststellen. Schließlich entnahmen die Forscher Gewebeproben und untersuchten Zellen im Detail. Einige Nervenzellen reagierten auf elektrische Reize, zum Teil zeigten Synapsen dieser Neuronen spontane Aktivität.
Vielversprechendes Hirnmodell
Für die Studienautoren belegen diese Ergebnisse, dass das Gehirn eine größere Kapazität für zelluläre Regeneration besitzt als bisher angenommen. Ob nach diesem Prinzip die Wiederherstellung normaler Gehirnfunktionen möglich wäre, bleibt aber unklar und wurde in der vorliegenden Studie auch nicht untersucht. Von unmittelbarer klinischer Bedeutung seien die Versuche zwar nicht, so Sestan. "Die zellschützende Rezeptur von Brainex könnte aber eines Tages in Therapien für Herz-Kreislauf-Erkrankungen Anwendung finden."
Vor allem aber dürften die Ergebnisse die Hirnforschung beflügeln, kommentierte Bernd Böttiger von der Universitätsklinik Köln die Studie, an der er nicht beteiligt war. "Ein solches Forschungsmodell wäre ein sehr mächtiges Experimentalsystem." Damit könnte künftig etwa untersucht werden, bis zu welchem Zeitpunkt nach einem Herz-Kreislauf-Stillstand eine normale Hirnfunktion wiederhergestellt werden kann. (David Rennert, 17.4.2019)