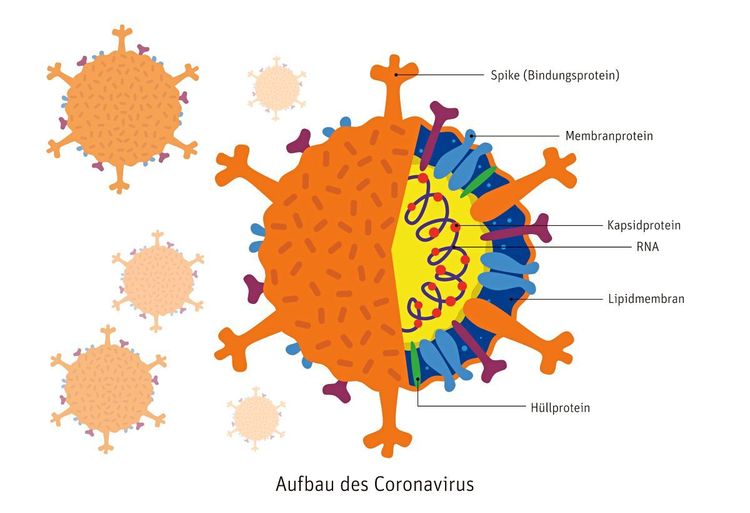
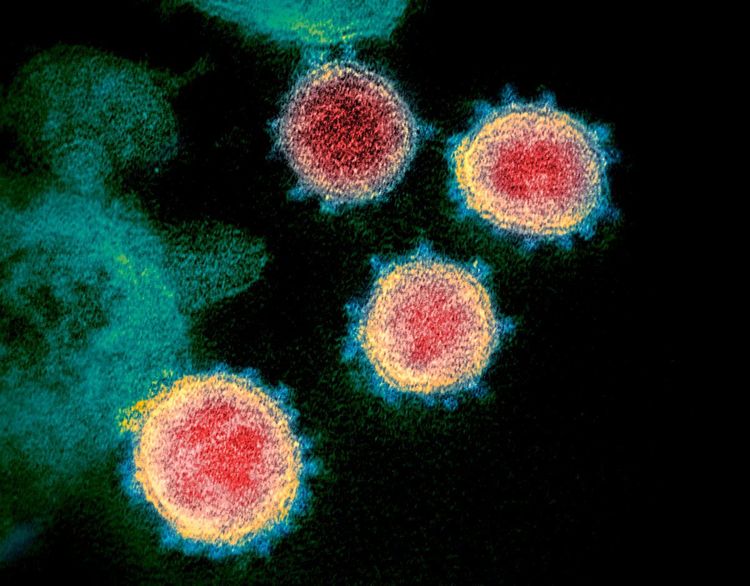
Der Name Coronavirus kommt nicht von ungefähr. Als Wissenschafter zum ersten Mal die Struktur eines Vertreters dieser Virusfamilie unter dem Elektronenmikroskop erblickten, mussten sie unweigerlich an kleine Kronen denken. Das war in den 1960er-Jahren – seither hat sich die Mikroskopie enorm weiterentwickelt und liefert heute ein anderes, besseres Bild. Statt zackiger Krönchen ähneln die Coronaviren eher Igelbällen, die für Massagen oder gegen Stress eingesetzt werden: Sie sind rund und haben viele stachelartige Strukturen an der Oberfläche. Der lateinische Ausdruck für Krone – Corona – ist ihnen aber geblieben.
Mehr als 40 Coronaviren sind heute bekannt, die eine Vielzahl von Säugetieren und Vögeln infizieren können. Lange Zeit beschäftigten sie vor allem die Veterinärmedizin, weil sie Krankheiten bei Schweinen, Rindern und Geflügel verursachen. Zwei Coronavirus-Arten lösen auch Erkältungssymptome beim Menschen aus – mit unangenehmen, aber ungefährlichen Folgen.
Von Fledermaus zu Mensch
Das änderte sich Ende 2002 schlagartig: Ein Coronavirus sprang damals von einer Fledermaus auf einen Menschen über, in der Folge infizierten sich weltweit Menschen damit und erkrankten am schweren akuten Atemwegssyndrom (Sars). Rund 800 Personen starben. 2012 tauchte zum zweiten Mal ein gefährliches Coronavirus auf, das vor allem auf der Arabischen Halbinsel grassierte: Mers, das von Dromedaren übertragen wurde. Mit Sars-CoV-2 ist nun einem weiteren Coronavirus der Sprung vom Tier auf den Menschen gelungen – und es verbreitet sich in einem unvergleichbaren Ausmaß um den Erdball.
Noch gibt es keine Impfungen und Medikamente, die der Infektion Einhalt gebieten können – genau daran forschen Wissenschafter auf Hochtouren. Derzeit laufen mehr als 40 Projekte zur Entwicklung von Impfstoffen. Bis Massenimpfungen verfügbar sind, wird es aber lange dauern. Die vordergründigen Hoffnungen richten sich daher auf Medikamente, mit denen sich die durch das Virus ausgelöste Lungenerkrankung Covid-19 behandeln lässt.
Pharmazeutische Abkürzung
"Die größten Chancen für schnelle Behandlungserfolge liegen im Drug-Repurposing", sagt Sylvia Knapp, Professorin für Infektionsbiologie an der Med-Uni Wien. Bereits zugelassene Medikamente werden dabei auf ihre Wirkung gegen Corona getestet – sie könnten weitaus schneller eingesetzt werden als neu entwickelte Präparate, die erst aufwendige Verfahren durchlaufen müssen. Die gute Nachricht: Da Coronaviren seit Jahrzehnten bekannt sind, ist ihre Biologie gut erforscht. Dieses Wissen verschafft Forschern einen Vorsprung bei der Frage, welche existierenden Medikamente gegen Sars-CoV-2 wirksam sein könnten.
Um zu verstehen, was die Wissenschaft in der Corona-Krise Hoffnung schöpfen lässt, bedarf es eines Blicks in die Substruktur von Sars-CoV-2. Ein Virion – so wird ein einzelnes Viruspartikel bezeichnet – misst etwa 90 Nanometer und ist damit um mehrere Größenordnungen kleiner als die Zellen, die es in der menschlichen Lunge infiziert. Es besteht aus vier Proteinen und einem RNA-Strang, der die genetischen Informationen des Virus trägt. Im Fall von Sars-CoV-2 sind das 29.900 Nukleotide, also codierte Bausteine, die das Programm zur Vervielfältigung des Virus beinhalten.
Suche nach Medikamenten
Das auffälligste Protein hat die Form stachelartiger "Spikes" in der Virushülle. Diese viralen Enterhaken sind für die Bindung an die Wirtszelle verantwortlich. Zwischen den Spikes sitzen ein Membranprotein und ein Hüllprotein, die für die Stabilität des Virions sorgen. Im Inneren der Hülle befindet sich ein Kapsidprotein, das den Bausteinen der RNA als Gerüst dient (siehe Grafik).
Das Wissen um die Beschaffenheit der Proteine des Coronavirus ist entscheidend, um passende Medikamente zu finden. Denn die Wirkungsweise von Pharmazeutika beruht letztlich immer darauf, bestimmte Proteinfunktionen entweder zu blockieren oder zu verändern. Dafür muss ein Wirkstoff gefunden werden, der durch seine molekulare Struktur genau in die Struktur eines bestimmten Proteins passt und dessen Funktion damit verändern oder ausschalten kann. Erschwert wird diese Suche dadurch, dass Proteine in der Regel hochkomplexe dreidimensionale Strukturen aufweisen. Noch dazu sind sie nicht starr, daher muss auch die Dynamik stimmen, damit sich ein Wirkstoffmolekül entsprechend einklinken kann.
Zelluläre Angriffsziele
Ein Angriffsziel auf die Corona-Infektion ist der sogenannte ACE2-Rezeptor, der tief in der Lunge in Epithelzellen liegt, sagt Infektionsbiologin Knapp. An ACE2 dockt das Virus mithilfe des Spike-Proteins an, um in die Lungenzellen zu gelangen. Der Rezeptor darf allerdings nicht deaktiviert werden, weil er bei akutem Lungenversagen, das ein zentrales Problem bei schweren Covid-19-Erkrankungen darstellt, eine sehr positive Rolle spielen kann.
Knapp hält den Ansatz, den das Wiener Biotechunternehmen Apeiron verfolgt, für vielversprechend: Das vom österreichischen Genetiker Josef Penninger gegründete Unternehmen hat im Zuge der Sars-Pandemie 2002/2003 ein biotechnologisch hergestelltes, lösliches ACE2-Protein entwickelt, das das Sars-Virus abfangen und Infektionen dämpfen konnte. Derzeit wird eine Studie zur Wirkung bei schwerem Lungenversagen durch Covid-19 vorbereitet.
Internationale Zusammenarbeit
Andere Ideen setzen ebenfalls beim Verhalten des Coronavirus im menschlichen Körper an. Um sich zu vermehren, muss es an Zellen anheften und in sie eindringen. Dafür verwendet das Spike-Protein neben ACE2 auch andere Enzyme wie die zelluläre Protease TMPRSS2, sagt Knapp. Auf dieses Enzym sind auch einige bereits getestete und freigegebene Medikamente gerichtet, etwa Camostat, das zur Behandlung chronischer Bauchspeicheldrüsenentzündungen eingesetzt wird. Erfolge erhofft man sich auch von Studien mit Remdesivir, einem gegen Ebola entwickelten Medikament, das sich als wirksam bei Sars- und Mers-Infektionen erwies.
Klinische Studien zu Wirksamkeit und Verträglichkeit braucht es natürlich trotzdem, ehe ein bereits zugelassenes Medikament für eine neue Erkrankung eingesetzt werden kann. Die internationale Zusammenarbeit vieler Forscher und Behörden gibt aber Hoffnung, dass dies in der aktuellen Ausnahmesituation mit höchster Priorität passiert. (David Rennert, Tanja Traxler, Peter Illetschko, 18.3.2020)