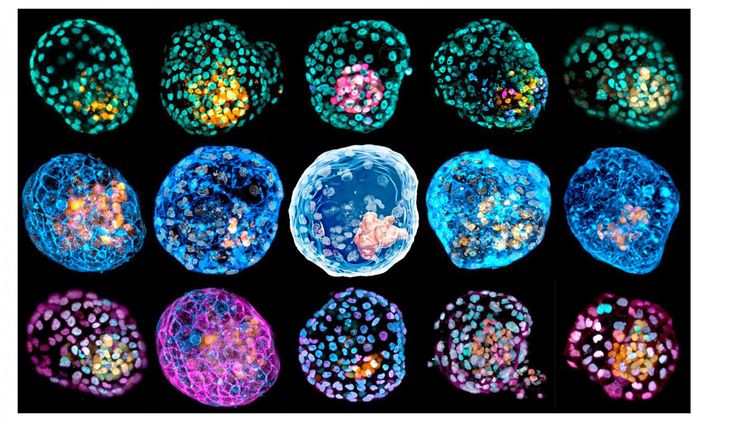
Embryoähnliche Zellstrukturen könnten dabei helfen, Fehlentwicklungen in der frühen Schwangerschaft besser zu verstehen.
Bei uns Säugetieren steht am Beginn der Entwicklung eines Embryos bekanntlich die Verschmelzung von Ei- und Samenzelle. Die befruchtete Eizelle beginnt sich zu teilen, schon nach wenigen Tagen entwickelt sich aus den Stammzellen die sogenannte Blastozyste. Wenn sich diese Zellstruktur in die Gebärmutterschleimhaut eingenistet hat, beginnt die Schwangerschaft – und aus der Blastozyste entstehen Plazenta und Fötus. Jetzt ist Wissenschaftern erstmals die Herstellung blastozystenähnlicher Strukturen aus menschlichen Zellen im Labor gelungen – ohne Befruchtung.
Wie zwei Forschergruppen aus den USA und Australien aktuell im Fachblatt "Nature" berichten, handelt es sich bei den künstlichen Gebilden, die Blastoide genannt werden, um Strukturen aus etwa 200 embryonalen Zellen. Sie ähneln Blastozysten, die etwa fünf bis sechs Tage nach einer natürlichen Befruchtung entstehen. Die Technik könnte die Erzeugung einzigartiger Modelle für die medizinische Forschung erlauben, die etwa für Studien zu frühen Entwicklungsdefekten oder zu Ursachen für frühen Schwangerschaftsverlust wertvoll wären.
Gewebe- und Stammzellen
Jose Polo und Kollegen von der australischen Monash University reprogrammierten für ihre Studie sogenannte Fibroblasten, also Zellen des Bindegewebes, und erzeugten daraus in einer 3D-Zellkultur Blastoide. Das US-amerikanische Team um Jun Wu vom University of Texas Southwestern Medical Center differenzierte unabhängig davon embryonale Stammzellen zu blastozystenähnlichen Strukturen aus. Beide Gruppen berichten von einer Erfolgsrate von maximal 20 Prozent. Die künstlichen Blastoide ähnelten nach Angaben der Studienautoren nach sechs bis acht Tagen in Größe, Form und Zellenanzahl natürlich entstandenen Blastozysten.
Die australische Gruppe führte zudem erste In-vitro-Einnistungsexperimente durch – die Blastoide wurden im Inneren einer Plastikschale versuchsweise zum Wachsen gebracht. Aus ethischen Gründen wurden diese Experimente nach viereinhalb Tagen wieder beendet. Aus rechtlicher Sicht sei das in Ordnung, sagte Jochen Taupitz, Direktor des Instituts für Deutsches, Europäisches und Internationales Medizinrecht an der Universität Mannheim, der nicht an den Studien beteiligt war.
Auch nach deutschem Recht sei die Erzeugung solcher zellulärer Strukturen zulässig und würde nicht vom Embryonenschutzgesetz erfasst, sagte Taupitz. "Das ist auch richtig so, weil sich aus ihnen kein ganzheitlicher Organismus entwickeln kann. Aber selbst, wenn dies in der Zukunft anders sein sollte, sollte ihre Erforschung in vitro jedenfalls bis zu dem Zeitpunkt, zu dem sich erste Strukturen von Empfindungsfähigkeit auszubilden beginnen, erlaubt sein." Dies sei bei Embryonen, die wie bei der natürlichen Zeugung durch Befruchtung entstehen, nach neueren Erkenntnissen jedenfalls bis etwa 28 Tage nach der Befruchtung nicht der Fall.
Vielfältige Modelle
Für Nicolas Rivron vom Institut für Molekulare Biotechnologie (IMBA) in Wien sind die neuen Ergebnisse ein weiterer Schritt zur Bildung eines menschlichen Blastozystenmodells. Rivron selbst hatte 2018 mit Kollegen erstmals blastozystenähnliche Strukturen aus Mäusezellen entwickelt. Wie sehr die nun vorgestellten menschlichen Zellstrukturen natürlichen humanen Blastozysten ähneln, müsse sich erst zeigen: "Die Morphologie der Blastoide in diesen Papieren ist in Ordnung, aber sie bilden sich sehr ineffizient und dreimal langsamer als Embryonen, was bedeutet, dass einige Elemente fehlen." Um ein realistisches Modell zu erzeugen, müssten noch viele Probleme ausgeräumt werden.
Die Vorteile solcher Modelle für die medizinische Forschung sind laut Rivron vielfältig: Erstmals könnten Wissenschaftern Modelle des frühen Embryos zur Verfügung stehen, die in großer Zahl produziert und auch leicht verändert werden könnten, um spezifischen Forschungsfragen nachzugehen. "Blastoide sind gute Modelle, die verwendet werden können, um zu verstehen, wie sich der Embryo entwickelt, und um Medikamente zu testen. Wir können uns also vorstellen, dass sie gute Plattformen sind, um neue Behandlungen zu entwickeln, um zum Beispiel Fehlgeburten oder Unfruchtbarkeit zu verhindern, indem man den Prozess der Einnistung verbessert", sagte der Forscher. (dare, 17.3.2021)