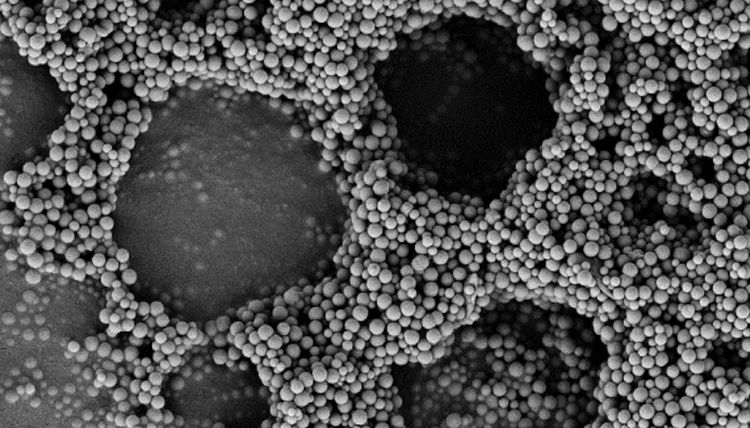
Die Rasterelektronenmikroskop-Aufnahme zeigt Strukturen, die an Bienenwaben erinnern. Peptide mit der Fähigkeit zur Selbstorganisation ordnen Kolloide zu neuen, größeren Strukturen an.
Peptide sind kleine Eiweiß-Bausteine, die dazu neigen, sich gleichsam aus eigenem Antrieb zu größeren Einheiten zusammenzuschließen. Diesen Umstand haben sich nun Wiener Chemiker zunutze gemacht, um mithilfe kurzkettiger Peptide aus kleinen Nanopartikeln gezielt größere Strukturen heranwachsen zu lassen. Bei der Methode fungieren die Eiweißmoleküle als eine Art Ordner und Klebstoff für die Nanopartikel. Der Ansatz könnte Grundlage für das Design neuartiger Materialien sein, berichten die Wissenschafter im Fachjournal "Angewandte Chemie".
Spontane Selbstorganisation
Die Wissenschafter von der Universität Wien um die Studienautoren Freddy Kleitz und Michael Reithofer nützen bei ihrem Ansatz das Phänomen der spontanen Selbstorganisation (Selbstassemblierung) von Molekülen. Bei den Siliziumdioxid-Nanopartikeln, die einen Durchmesser von rund 100 Nanometern haben, stellt sich der Effekt allerdings nicht von selbst ein. Die Wissenschafter setzen daher auf bestimmte Anhängsel, die sich sehr wohl selbst organisieren.
Im speziellen Fall wählten die Forscher den Zugang, Diphenylalanin-Peptide chemisch an Nanopartikel anzubinden, die sich verteilt in einem organischen Lösungsmittel befinden, "welches wenig Einfluss auf die Selbstorganisation hat", sagte Reithofer. Tatsächlich haben die Peptide "die Selbstorganisation angeleitet: Sie können die Oberfläche der kleinen Teilchen ummanteln und die Partikel dann – wie bei einem Klettverschluss – zusammenhalten". Man könne also über die Peptide die Nanopartikel zusammenhalten und organisieren, so der Forscher.
Einfluss auf die Strukturen
Das gelang den Wissenschaftern, indem sie das Lösungsmittel verdampften, in dem sich die Nanopartikel und ihre Peptid-Anhängsel befanden. Der Clou dabei ist, dass man beeinflussen kann, welche größere Struktur entsteht. Als wichtigste Stellschrauben identifizierten die Forscher die Art der Lösungsmittel selbst und wie rasch diese verdampft werden.
Je nach Bedingungen lässt der Organisationsdrang der Peptide die Siliziumdioxid-Nanopartikel in anderen Konstellationen zueinanderfinden. So offenbarten detaillierte Analysen etwa bienenwabenartige Strukturen mit verschiedenen Lochgrößen, für die die Bildung von verschieden großen Wassertropfen beim unterschiedlich raschen Verdampfen verantwortlich zu sein scheint.
Materialien mit verschiedensten Anwendung
Neben dem Diphenylalanin untersucht die Gruppe nun auch den Einfluss anderer Peptide. Mit dem neuen Ansatz stehe man zwar noch am Beginn der Entwicklungsarbeit, die Methode öffne aber eine Tür, "eine große Anzahl an verschiedenen Materialien zu designen – auch im Hinblick auf verschiedenste Anwendung wie etwa Wirkstofftransportsysteme oder neuartiger Nanokatalysatoren", erklären die Forscher. (red, APA, 2.10.2021)