Nein, man könne ihr keine Stammzellen vorbeibringen, um daraus ein Herz zu züchten. Wenn Viktoria Weber, Vizerektorin für Forschung und nachhaltige Entwicklung sowie Leiterin des Departments Biomedizinische Forschung an der Universität Krems, in die Zukunft blickt, bleibt sie realistisch, weiß aber gleichzeitig: "Mit Forschung und Entwicklung betritt man ständig Neuland."

Das trifft ganz besonders auf die Entwicklung künstlicher Organe und Organteile zu, woran seit Jahrzehnten mit Nachdruck und in viele Richtungen geforscht wird. Deutlich wurde das nicht zuletzt auf der kürzlich abgehaltenen Jahrestagung der European Society for Artificial Organs (ESAO), die von 6. bis 10. September in Krems stattfand.
Multidisziplinärer Ansatz
"Unsere knapp 450 Mitglieder aus 38 Ländern beschäftigen sich nicht nur mit künstlichen Organen, sondern auch mit Organersatz, Organunterstützung und der Regeneration von Organen", erklärt Weber, die neben ihrer leitenden Funktion an der niederösterreichischen Universität derzeit auch Präsidentin dieser wissenschaftlichen Vereinigung ist.
Weltweit sei der Bedarf an künstlichen Organen hoch, sagt Weber: "Die Wartelisten für Transplantationen sind lang, und die demografische Entwicklung wird den Bedarf weiter erhöhen." Als mögliche Lösung gelten Xenotransplantationen, also der Organersatz aus der Tierwelt. Zwar gelang kürzlich an der Universitätsklinik in Baltimore die weltweit erste Transplantation eines genetisch modifizierten Schweineherzens. Der Patient überlebte zwei Monate. "Bei der Xenotransplantation sind jedoch noch viele Fragen offen", warnt Weber vor überzogenen Erwartungen. Neben der Gefahr einer Virenübertragung sowie Abstoßungsreaktionen müssten auch noch zahlreiche ethische Fragen geklärt werden.
Als anderer Lösungsansatz gilt die Herstellung von Organen im Labor mittels "Tissue-Engineering". Dabei werden Stammzellen oder Gewebezellen eines Patienten vervielfältigt und in einem Bioreaktor zu einem neuen Organ entwickelt. Der an der Harvard Medical School forschende Österreicher Harald Ott konnte schon vor zehn Jahren einer Ratte einen im Bioreaktor gezüchteten Lungenflügel einsetzen. Das Tier atmete damit fünf Tage lang.
Mühseliger Fortschritt
Die Entwicklung ist seither aber nicht mit derselben Dynamik und Geschwindigkeit weitergegangen. Für die Rekonstruktion eines kompletten Organs müssen noch viele Einzelschritte gelöst werden. Dazu zählt das zentrale Problem der Vaskularisierung, also der Bildung kleiner und kleinster Blutgefäße. Ohne diese kann das Zellgewebe nicht durchblutet werden und stirbt unweigerlich ab. Als große Herausforderung gilt, dass schon allein das erforderliche Zusammenspiel der verschiedenen spezialisierten Zellarten für die Neubildung von Blutgefäßen bisher nicht vollständig verstanden wird.
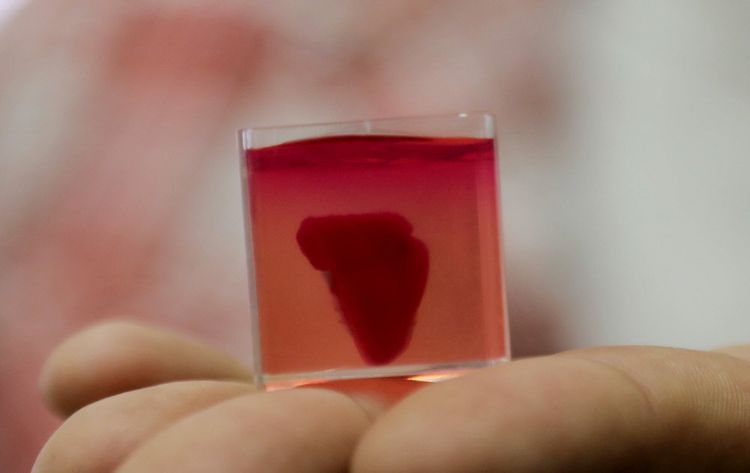
Dafür könnten "Miniorgane", sogenannte Organoide, bald vermehrt in der Forschung eingesetzt werden. Die wenige Millimeter großen Organoide besitzen ein enormes Potenzial für die Erforschung von Krankheiten. Aber auch für die Entwicklung und Testung neuer Medikamente sowie für die Untersuchung der Organentwicklung gelten sie als große Zukunftshoffnung. Viele Fragestellungen könnten damit oftmals sogar besser untersucht werden als im Tiermodell.
Insgesamt geht es Weber zufolge derzeit weniger um disruptive Durchbrüche als um kontinuierliche Innovationen. Das sehe man etwa auch bei der Dialyse: Während der erste Dialysefilter für die Blutentgiftung bei Nierenversagen in den 1940er-Jahren noch "fast so groß wie eine Badewanne war", sind Dialysefilter heute hocheffizient und flächendeckend verfügbar, erklärt Weber. Aber selbst hier gebe es Raum für Weiterentwicklungen. Zwar sind Nebenwirkungen der Dialyse heute deutlich geringer, weil die Filter wesentlich blutverträglicher geworden sind, dennoch stellen chronische Entzündungsreaktionen immer noch einen kardiovaskulären Risikofaktor dar.
Ähnlich wie bei der Dialyse kann mittlerweile auch die Entgiftungsfunktion der Leber maschinell simuliert werden. Damit kann etwa die Zeit überbrückt werden, bis ein geeignetes Spenderorgan zur Verfügung steht. Die Simulation anderer Leberstoffwechselfunktionen mit bioartifiziellen Systemen, etwa mithilfe von Leberzellen im Bioreaktor, hat sich aufgrund ihrer Komplexität bisher allerdings nicht durchsetzen können.
Hoffen auf Kunstherzen
Erfolgreich etabliert hat sich indes die Kunstherzforschung. Komplette Kunstherzen kommen zwar selten zum Einsatz. Mit Herzunterstützungssystemen, die die Pumpleistung von linker oder rechter Herzkammer erhöhen, können Patienten heute jedoch schon jahrzehntelang überleben. Auch diese Systeme werden laufend weiterentwickelt und mit entsprechender Sensorik ausgestattet, die den Gesundheitsstatus des Patienten überwachen. (Norbert Regitnig-Tillian, 18.9.2022)